
遺傳基因的命運將阿茲海默症降臨在龐大的哥倫比亞家族中,但這個家族有一名女性逃過了詛咒,她的逃脫或許是阻止乃至預防阿茲海默症的關鍵。
遺傳性阿茲海默症通常在40歲左右開始侵蝕患者的腦部,主因是一種名為「早老素-1」的基因發生突變導致失智,最終連生活也無法自理。哥倫比亞麥德林附近的居民稱這種疾病為「la bobera」,意思是「愚蠢、癡呆」。
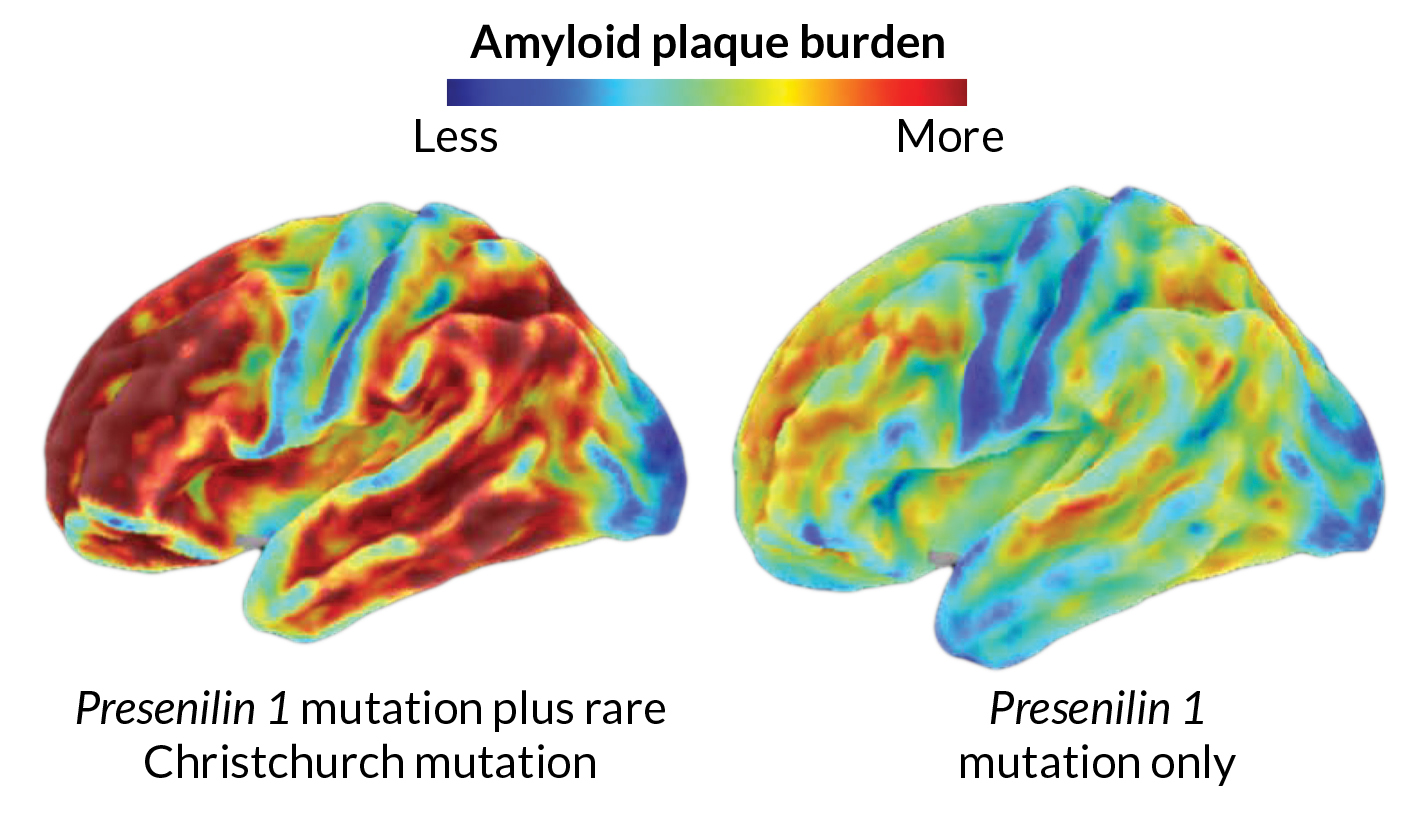
這個家族裡有一名女性同樣攜帶導致失智的突變基因,但不知為何她抵禦了阿茲海默症。她的大腦充滿類澱粉蛋白所形成的斑塊,許多科學家認為類澱粉蛋白的沉積是阿茲海默症發病的最早跡象之一。然而,直到70多歲以前,這名女性頭腦依然很敏銳。
科學家被這個情況難倒了,直到他們發現這名女性還攜帶了另一種極其罕見的突變基因,似乎保護她免受第一種突變的影響。哈佛醫學院細胞生物學家約瑟夫‧阿波列達-貝拉斯克斯(Joseph Arboleda-Velasquez)指出,第二種突變是在另一種與阿茲海默症相關的載脂蛋白E(ApoE)中所發生,它似乎能將阿茲海默症的發展速度延緩數十年,他說:「當時認定類澱粉蛋白沉積導致阿茲海默症為必然的結果,但這名女性的情況帶來了不同的觀點。」
阿波列達-貝拉斯克斯與同事在《自然醫學》(Nature Medicine)期刊上提及這名女性身上的特殊情況,但為了保護隱私省略了其姓名和確切年齡。

儘管這個發現目前只找到一個案例,但它表明退行性疾病也有弱點。據估計,單在美國就有580萬人受退行性疾病的影響。目前為止,幾乎所有希望減緩或阻止這類疾病的臨床實驗都以失敗告終,促使失望的科學家擴大研究尋找有效的治療方法。
也許,這位逃離詛咒的哥倫比亞女性具有某種能阻止阿茲海默症的方法,或至少延緩發病時間,阿波列達-貝拉斯克斯說:「我們是否能研發出一種藥物,對沒有攜帶第二種突變基因的人也有效呢?這方面的潛力巨大無窮。」
絕大多數的阿茲海默症是偶然發生,沒有明確的遺傳病因,病患通常在阿茲海默症發病以前就已經是七、八十歲的老年人,但更早發病的突變並不尋常,例如在這個哥倫比亞家族中所發現的「派薩突變」(Paisa mutation)。然而,儘管它們的起源與發並時間不同,但這兩種阿茲海默症都有類似的發展方式。
一般來說,早老素-1會生成蛋白質幫助分解黏稠的類澱粉蛋白,由此所產生的片段被稱為「β類澱粉蛋白」,並且無害地從大腦排出。然而,哥倫比亞家族中所發現的早老素-1突變基因在分解過程時產生了糾纏,導致大量的類澱粉蛋白在腦細胞之間沉積形成斑塊。
在20多歲攜帶這種突變基因的人所進行的腦部掃描中,這種沉積現象已經顯現出來。到45歲左右,許多人開始有記憶障礙;通常在50歲時發展成完全失智的狀態。
遺傳到一個突變副本就足以導致過量的類澱粉蛋白沉積,並導致阿茲海默症。美國國家老齡化研究所所長、免疫學專家理查‧霍德斯(Richard J. Hodes)認為,這種突變對這個家族的巨大影響是「類澱粉蛋白為阿茲海默症發病關鍵的有力論據之一」。
這個哥倫比亞大家族約有5000名成員,包括約1000名攜帶派薩突變的成員。他們對於疾病研究相當寶貴,讓科學家得以接觸數百名已知的阿茲海默症高危險族群,從而研究阿茲海默症的發展過程(特別是初期階段),並從大腦和血液觀察阿茲海默症的初期徵兆。霍德斯指出,這名女性的家人竭盡全力幫忙,他們「步行或騎腳踏車到最近的公車站,然後搭公車轉乘火車,花好幾個小時到診所檢查」。
霍德斯最近訪問麥德林時,一位居民表示疾病已經是他們生活的一部分,他說:「如果我得到這種病,我知道我的家人,我的兄弟姊妹會照顧我。如果我有幸沒有得病,我也會照顧他們。」
當哥倫比亞科學家得知這名女子直到70多歲仍保持敏銳的頭腦時,他們安排她在家人與研究助理的陪同下,在2016年夏天遠赴波士頓檢查。哈佛醫學院的神經成像研究員亞克‧基羅斯(Yakeel T. Quiroz)和同事用腦部掃描儀器衡量她的類澱粉蛋白與大腦健康指標的其他數據,其中包括另一種與阿茲海默症相關、會在神經細胞內部糾纏的濤蛋白(Tau proteins)。
基羅斯表示,掃描顯示出她的大腦充滿著類澱粉蛋白,很可能已經沉積了數十年之久。常用來量化大腦類澱粉蛋白的評量表上,她的分數為1.96,遠高於1.2的正常數值,基羅斯說:「她的分數是我們見過的所有掃描對象中最高的人。」
基因分析顯示,這名女性的兩個載脂蛋白E基因副本都發生了「基督城基因突變」(以首次發現的紐西蘭城市命名),而進一步的檢測表明,這使她免受阿茲海默症的侵擾。霍德斯指出,這名女性的大腦存在大量的類澱粉蛋白,但她直到70多歲才開始出現症狀,這個事實「令人驚訝和耐人尋味,而且對研究可能非常有幫助」。
科學家需要做更多的研究,才能證實載脂蛋白E的基督城基因突變保護了她的大腦。但霍德斯認為,研究結果表明了一個簡單的事實:類澱粉蛋白本身不一定能導致失智。
在哥倫比亞家族以外的研究也發現,類澱粉蛋白並不代表全部真相,因為其他細胞因子也可能讓神經細胞死亡和記憶喪失,從而引發阿茲海默症。許多研究表明,神經細胞堵塞、濤蛋白糾纏與其他大腦疾病跡象與大腦衰退密切相關。這項研究對住在明尼蘇達州羅切斯特市的480名60歲以上老年人進行觀察,其結果反映了上述觀點。
這些參與者都沒有表現出阿茲海默症的跡象,而且都是隨機挑選來參加研究。為了找出哪種大腦變化最能預測往後的失智,梅奧醫院神經放射學家克里夫‧傑克(Clifford R. Jack Jr.)和同事測試了參與者的記憶表現,同時測量他們的類澱粉蛋白程度和其他大腦數據。該研究團隊於2019年6月在《美國醫學會期刊》(JAMA)發表的論文稱,類澱粉蛋白似乎與5年左右的記憶力衰退密切相關。
如果排除另外兩個令人頭疼的標記——濤蛋白糾纏或大腦萎縮——類澱粉蛋白並不能預測失智。換句話說,類澱粉蛋白可能只是製造機會,但它把真正發病的時機交給別的物質,傑克說:「大腦的類澱粉蛋白是最終導致阿茲海默症全面爆發的第一個階段,但在類澱粉蛋白沉積的初期階段到症狀發展之間還有很長一段時間。」

在哥倫比亞家族的案例中,這種間隔大約為10至15年的時間。對於零星的阿茲海默症患者來說,情況大致上也是這樣。但在《自然醫學》論文裡的那位女性,她延後發病的時間似乎是其他成員的兩倍之久。南加州大學阿茲海默症治療研究所所長保羅‧艾森(Paul Aisen)說:「這表明人們是有可能跟類澱粉蛋白相安無事共存數十年,而不是只有15年,這個發現令人興奮。」
這名女性的基因突變保護作用似乎源自一種極其特殊的變化,在基督城基因突變中載脂蛋白E的一個節點被調整了,而由此產生的蛋白質含有絲胺酸,取代了平常產生的精胺酸。
這種替換阻止載脂蛋白E與一些多醣蛋白結合,這些多醣蛋白被稱為硫酸類肝素(HSPGs),過去的研究表明,硫酸類肝素可能促進了類澱粉蛋白的沉積,並驅使神經細胞吸收更多有害的濤蛋白。
但是,為了表現出失常,硫酸類肝素可能必須跟載脂蛋白E結合。科學家懷疑,基督城基因突變很可能透過干擾這種有害關係來保護這位女性的大腦。但如果載脂蛋白E和硫酸類肝素之間失去特定的關聯,阿波列達-貝拉斯克斯說:「疾病的發展就會陷入停滯,就真的讓一連串事件畫上句點。」
載脂蛋白E作為阿茲海默症最重要的遺傳風險因子,長期以來一直被認為是阿茲海默症藥物的潛在靶點,而攜帶載脂蛋白E4基因的人罹患阿茲海默症的風險更高。
基羅斯、阿波列達-貝拉斯克斯和同事發表的初步研究報告指出,載脂蛋白E2能顯著降低這種風險;載脂蛋白E3通常帶來阿茲海默症的中等風險,但還有一個顯著的例外,那就是哥倫比亞婦女所攜帶的基督城突變基因。
在一般群體中,年齡是阿茲海默症的最大危險因子。隨著老齡化的趨勢增長,失智老人的數量也會激增。據估計到2050年時,美國將有1380萬人失智,全世界估計有5000萬人,而阿茲海默症會是失智的主因。
這個哥倫比亞家族仍繼續提供協助,讓科學家深入瞭解阿茲海默症的發展過程與可能的治療方法,基羅斯表示,阿茲海默症病患的家屬(包括哥倫比亞家族)不一定關心導致疾病的關鍵,他說:「他們更在乎有什麼能幫助患者改善病情,這才是患者與家屬所期待的事情。」
原文出處:Science News











 最新文章
最新文章 主題總覽
主題總覽 成為粉絲
成為粉絲 追蹤IG
追蹤IG 追蹤推特
追蹤推特 也有串串
也有串串 合作提案
合作提案